для чего разбирают старые автомобильные батареи, сколько кг свинца в АКБ
 Современные автомобильные аккумуляторы содержат свинец, сдав который, можно неплохо заработать, что позволяет несколько сократить затраты автовладельца на покупку новой батареи в автомобиль. Из соответствующих таблиц можно с легкостью определить, сколько свинца в аккумуляторе 55 и как добыть такой дорогостоящий металл, который можно в последующем сдать в пункты вторсырья.
Современные автомобильные аккумуляторы содержат свинец, сдав который, можно неплохо заработать, что позволяет несколько сократить затраты автовладельца на покупку новой батареи в автомобиль. Из соответствующих таблиц можно с легкостью определить, сколько свинца в аккумуляторе 55 и как добыть такой дорогостоящий металл, который можно в последующем сдать в пункты вторсырья.
Для чего извлекают свинец из АКБ
 В первую очередь необходимо определиться с тем, для чего же извлекают из аккумуляторов свинец. Этот металл сплав хорошо ценится в пунктах приема цветных металлов, что позволяет даже с одного автомобильного аккумулятора получить неплохую денежную сумму. Свинец — это тяжеловесный металл, который используется многими рыболовами для изготовления грузил и различных снастей. Поэтому редко какой рыбак откажется от возможности самостоятельно разобрать АКБ и найти необходимый ему дорогостоящий тяжёлый металл.
В первую очередь необходимо определиться с тем, для чего же извлекают из аккумуляторов свинец. Этот металл сплав хорошо ценится в пунктах приема цветных металлов, что позволяет даже с одного автомобильного аккумулятора получить неплохую денежную сумму. Свинец — это тяжеловесный металл, который используется многими рыболовами для изготовления грузил и различных снастей. Поэтому редко какой рыбак откажется от возможности самостоятельно разобрать АКБ и найти необходимый ему дорогостоящий тяжёлый металл.
Также старые свинцовые пластины-электроды используют для изготовления простейших аккумуляторов и источников питания различных устройств и бытовых приборов. Этот металл может перетираться в стружку, после чего его добавляют в краску или лаки, что не только позволяет придать поверхности оригинальную текстуру, но и обеспечивает максимально возможную стойкость, устойчивость к ультрафиолету и механическую прочность.
Устройство автомобильных аккумуляторов
Большинство людей уверены, что находящиеся внутри аккумулятора пластины-электроды выполнены из чистого свинца. Однако в действительности чистого металла в них содержится
Поэтому со стандартного автомобильного аккумулятора удается добыть двух-трехкилограммовый слиток дорогого металла.
Необходимо лишь определиться с тем, сколько килограммов свинца в аккумуляторе 60 ампер, а исходя из этого, и можно будет рассчитать полученное количество дорогого металла.
В процентном соотношении состав автомобильного АКБ будет выглядеть следующим образом:
- Электролит — около 20% от общей массы АКБ.
- Пластиковый корпус, перегородки и другие элементы из пластика — не более 10% всей массы.
- Свинец, диоксиды, оксиды и другие сплавы — около 60% веса.
Для большей наглядности, чтобы определиться тем, сколько свинца в автомобильном аккумуляторе, можно рассмотреть состав 55-амперной автомобильной батареи. Стандартный вес такой АКБ не превышает 15 кг. Пластика тут около 1,5 кг, 3 кг электролита и 10 кг металла. Чистого металла в АКБ будет содержаться не больше 3 кг.
Следует учитывать также тот факт, что полностью выплавить ценный металл из электродов бывает затруднительно, соответственно количество получаемого свинца будет ещё ниже.
Содержание этого ценного металла во многом зависит от мощности аккумулятора и его емкости. Если в 55-амперной АКБ будет содержаться около 3 кг чистого свинца, то уже в мощной батарее для грузовых автомобилей, которая выдает ток на уровне 150−190 Ампер-часов, может содержаться 9 кг этого металла. Исходя из данных таблиц можно с легкостью рассчитать, сколько килограммов свинца, который можно выплавить из электродных пластин, в аккумуляторе 55.
Как разобрать старую батарею
Изначально разборными были лишь аккумуляторы, которые изготавливались в Советском Союзе. Делалось это для того, чтобы у автовладельцев имелась возможность отремонтировать АКБ, заменив те или иные вышедшие из строя элементы.
А вот на западе наибольшей популярностью пользовались необслуживаемые аккумуляторы, которые не подразумевали возможности разборки батарей.
Большинство используемых сегодня аккумуляторов относятся к категории необслуживаемых, соответственно появляются определенные проблемы с тем, чтобы разобрать старую АКБ.
Для такой работы потребуется следующее:
 Защитные очки и резиновые перчатки.
Защитные очки и резиновые перчатки.- Лобзик по металлу.
- Пассатижи.
- Болгарка.
- Плоская отвертка.
- Молоток.
- Зубило.
- Паяльник высокой мощности.
- Дрель.
Выполняя такую разборку старого АКБ, необходимо соблюдать максимальную осторожность. Внутри батареи находится электролит, который при попадании на кожу или слизистые может вызвать химические ожоги. Поэтому следует обязательно надевать очки и защитные резиновые перчатки. Проделав соответствующие отверстия в банках, следует обязательно слить электролит и промыть дистиллированной водой батарею, в которой может также остаться соляная кислота.
Чтобы слить электролит, потребуется выкрутить пробки, а если таковые в АКБ отсутствуют, то самостоятельно дрелью выполняется отверстие, через которое и сливается жидкость. Такие отверстия для слива электролита лучше всего выполнять снизу аккумулятора, что позволит, не наклоняя батарею и не поднимая со дна выпавший осадок, слить всю соляную кислоту.
После промывки банок чистой водой следует, вооружившись лобзиком или болгаркой, отпилить крышку по периметру корпуса батареи. Достают крышку, на которой будут закреплены аккумуляторные пластины.

Если крышку и пластины держат приводные клеммы, то потребуется вручную с помощью молотка или зубила извлечь металлические электроды.
Самостоятельное получение свинца
Свинец плавится при невысоких температурах, соответственно провести выплавку этого металла из аккумуляторных электродов можно в домашних условиях на электрической или газовой плите. Однако в таких условиях можно расплавить металл, который находится в чистом виде. То есть потребуется использовать решетку, мостики и клеммы от АКБ.
А вот если требуется расплавить пластины и получить из них чистый свинец, то следует работать на температурах около 1000 градусов и использовать специальные химические реагенты.
Именно по причине такой сложности выплавки свинца в домашних условиях получить из аккумулятора даже несколько килограммов этого чистого тяжелого металла будет затруднительно. Поэтому зачастую бывает куда проще и выгоднее сдать старый аккумулятор в соответствующие пункты приёма вторсырья или специализированные компании, а не пытаться самостоятельно разобрать и выплавить дорогостоящий металл из электродов и других элементов АКБ.
Целесообразно ли выплавлять свинец самостоятельно
До недавнего прошлого сдать аккумулятор в переработку было затруднительно, поэтому многие экономичные автовладельцы самостоятельно позанимались разборкой АКБ и последующей сдачей дорогостоящего металла в пункты вторсырья. Сегодня же можно с легкостью сдать аккумулятор в специализированные конторы и не заниматься самостоятельно трудоемкой работой по выплавке свинца, тем более что в домашних условиях провести качественную очистку металла будет проблематично.
Современные АКБ в зависимости от своего типа, ёмкости и мощности могут содержать от 1 до 10 кг свинца. Если отдельные элементы полностью состоят из этого дорогостоящего металла, и переплавить их самостоятельно в домашних условиях не представляет сложности, то вот расплавить пластины, где свинец содержится в оксидах и гидроксидах, бывает затруднительно.
Поэтому проще всего сдать аккумулятор в пункты приема вторсырья, что позволит не только избавиться от необходимости сложной переплавки металла, но и получить неплохое денежное вознаграждение.
proakkym.ru
Электромобили спровоцировали борьбу за металлы – ВЕДОМОСТИ
Австралия – крупнейший в мире производитель лития, спрос на который, особенно в Китае, быстро растет из-за развития сектора электромобилей
Carla Gottgens / Bloomberg
Прогнозируемый рост мирового спроса на электромобили заставляет автопроизводителей озаботиться наличием сырья для выпуска аккумуляторов. К нему относятся литий, никель, кобальт, графит и редкоземельные металлы. Поэтому производители электромобилей и аккумуляторов стремятся обеспечить их поставки, договариваясь с горнодобывающими компаниями.
По данным Международного энергетического агентства (МЭА), в прошлом году в мире было 2 млн электромобилей. К 2040 г. их число достигнет минимум 40 млн, прогнозирует МЭА. И крупнейшие горнодобывающие компании уже начали менять свой бизнес, чтобы обеспечить поставку материалов для литий-ионных аккумуляторов. Нынешний год должен стать «переломным моментом» для электромобилей, заявила BHP Billiton.
В сентябре китайский автопроизводитель Great Wall Motor подписал соглашение с австралийской Pilbara Minerals об обеспечении себе поставок лития на пять лет. В октябре другая австралийская горнодобывающая компания, Galaxy Resources, сообщила, что ведет переговоры о долгосрочных поставках лития с несколькими производителями автомобилей и аккумуляторов. В их число входит Panasonic, выпускающая аккумуляторы для Tesla. «Это подчеркивает, какое стратегическое значение для мировой автомобильной промышленности приобретает доступ к крупным, надежным и высококачественным источникам материалов для аккумуляторов в странах с низким риском», – заявил гендиректор Pilbara Кен Бринсден.
Спекулянты тоже не остаются в стороне, так как эти металлы сильно дорожают; их возросшая активность на рынке еще больше толкает цены вверх. Инвесткомпания Cobalt 27 уже закупила более 2000 т кобальта. Этот металл подорожал более чем на 190% за последние полтора года. Обеспечить поставки кобальта труднее всего, поскольку 65% его добычи приходится на Демократическую Республику Конго (ДРК), одну из беднейших стран мира. По прогнозам аналитиков UBS, спрос на кобальт удвоится к 2020 г. примерно до 200 000 т в год. Поэтому потребуются новые проекты, чтобы избежать его дефицита в долгосрочной перспективе. «Без кобальта из ДРК вообще нельзя будет говорить о производстве электромобилей – вот насколько рынку нужно больше этого металла», – утверждает Саймон Мурс из Benchmark Mineral Intelligence.
Литий хоть и более доступен, но в ближайшие годы тоже может возникнуть нехватка его предложения. Спрос на литий вырастет в четыре раза до 779 000 т к 2025 г., по оценкам Goldman Sachs. Но удовлетворить его будет трудно, так как «многие проекты, которые были анонсированы с фанфарами, не смогли привлечь достаточного финансирования», отмечают аналитики банка. Литий сейчас добывается в горах Австралии и пустынях Южной Америки. Но не все его запасы пригодны для производства аккумуляторов, отмечает гендиректор Neo Lithium Вальдо Перес. Например, у Боливии огромные запасы лития, но они содержат много примесей магния. Поэтому «Боливия определенно не подходит», говорит Перес.
Главную неопределенность для сырьевых рынков представляет то, какой будет технология выпуска аккумуляторов. Их производители сокращают использование кобальта из-за высокой цены и проблем с поставками. В сентябре британская Johnson Matthey заявила, что разработала более эффективные аккумуляторы с использованием лития и никеля и меньшим содержанием кобальта. Как отмечает инвестбанк Liberum, никель помогает повысить мощность аккумуляторов и при этом стоит в шесть раз дешевле кобальта, а его предложение примерно в 20 раз выше. По прогнозам Мурса из Benchmark Mineral Intelligence, спрос на никель вырастет с 75 000 т в 2016 г. до 400 000 т к 2025 г.
В долгосрочной перспективе производители аккумуляторов намерены изменить их конструкцию. Британская Dyson планирует выйти на рынок электромобилей к 2020 г. с помощью твердотельных аккумуляторов, которые должны хранить и отдавать больше энергии. Toyota тоже стремится начать использовать твердотельные аккумуляторы в своих автомобилях в начале 2020-х гг. Они заменят аккумуляторы с жидким электролитом.
«Всем хочется в будущем иметь чудесные химические вещества, не связанные с этими редкими материалами, но сейчас они недоступны, – говорит Стивен Айриш из британской Hyperdrive, занимающейся аккумуляторами. – Все задаются вопросом, произойдет ли революция в производстве аккумуляторов. Но на самом деле речь идет о серии постепенных улучшений».
Самые продаваемые автомобили на электрической тяге
www.vedomosti.ru
Материалы, используемые в аккумуляторах (батареях)
- Категория: Поддержка по аккумуляторным батареям
- Опубликовано 22.04.2016 01:45
- Автор: Abramova Olesya
В электрических батареях используются разнообразные химические элементы, добываемые из земной коры. Забавно то, что ровно такие же элементы входят в состав всех живых существ на нашей планете. Как и в живом организме, вещества для электрических батарей должны быть тщательно подобраны в нужном количестве, чтобы достичь гармоничного взаимодействия. Превышение количества всего лишь одного материала может испортить весь тонкий баланс.
Алюминий (Al) представляет собой мягкий, серебристо-белый, немагнитный металл. Добытый из бокситов, он является третьим наиболее распространенным элементом в земной коре после кислорода и кремния. При контакте с воздухом алюминий образует пассивирующий слой, который защищает металл от коррозии. Алюминий используется в качестве материала катода в некоторых версиях литий-ионных аккумуляторов [BU-205].
2. Ванадий
Ванадий (V) является очень твердым металлом серебристого цвета. Он был обнаружен в 1801 году в Мексике, находится в составе 65 минералов и образует устойчивый слой оксида на своей поверхности. Крупнейшими производителями ванадия являются Китай и Россия. Этот металл используется в специальных сплавах, а в сфере электрохимических источников энергии он востребован в проточной [BU-210b] конструкции аккумуляторов.
3. Железо
Железо – это наиболее распространенный по массе элемент на нашей планете. Химическое обозначение Fe происходит от латинского слова “ferrum”. Железо использовалось человечеством еще с незапамятных времен, хотя медные сплавы с более низкой температурой плавления существовали еще раньше. Чистое железо является достаточно мягким, и может быть укреплено с помощью создания сплава с углеродом. Соединения железа играют важную роль в биологии. В сфере электрических батарей железо нашло свое применение в литий-железо-фосфат-оксидной [BU-205] электрохимической системе.
4. Кадмий
Кадмий (Cd) является мягким синевато-белым металлом. Обнаруженный в 1817 году в Германии, кадмий являлся побочным продуктом при производстве цинка, и использовался в основном как добавка к стали для предотвращения коррозии. Сейчас кадмий используется как материал для анода в никель-кадмиевых батареях [BU-203], но так как он является токсичным материалом, во многих странах его использование запрещено.
5. Кальций
Кальций – это мягкий металл щелочной группы серого цвета. Его химическое обозначение — Са. Он был обнаружен английским химиком Хэмпфри Дэви в 1808 году. Это пятый самый распространенный по массе элемент в земной коре; он играет важнейшую роль для живых организмов, так как отвечает за формирование таких органов как кости, зубы и раковины. Кальций повышает производительность и механическую прочность свинцовых пластин в свинцово-кислотных электрических батареях.
6. Марганец
Марганец (Mn) добывается вместе с железом и другими полезными ископаемыми. Он назван в честь древнегреческого города Магнесия, возле которого был найден черный минерал, содержащий этот металл. Марганец используется для предотвращения коррозии железа, а также служит в качестве катодного материала для литий-ионной [BU-205], угольно-цинковой [BU-106] и щелочной [BU-106] электрохимических схем.
7. Натрий
Натрий (Na) — мягкий, серебристый, химически активный металл, который принадлежит к группе шести элементов с одним электроном на внешней оболочке. Теряя электрон, атом натрия становится положительно заряженным. Натрий является шестым самым распространенным элементом в земной коре, но доступен лишь в виде соединений. Он впервые был выделен Хэмпфри Дэви в 1807 году путем электролиза гидроксида натрия. Соединения натрия используются в производстве мыла и антиобледенительных веществ, но самым знаковым его применением является использование хлорида натрия, или по простому — кухонной соли. Натрий также является очень важным элементом для всех живых существ и растений. В сфере электрических батарей натрий используется в серно-натриевых [BU-210a] батареях.
best-energy.com.ua
Сколько свинца в аккумуляторе
Отслуживший автомобильный аккумулятор это источник чистого свинца, многие его сдают, другие пытаются разобрать и переплавить и тут возникает справедливый вопрос – а сколько этого металла в строении самой батареи ведь вес больших вариантов может достигать до 40 и более килограмм? Если смысл самому переплавлять и сдавать уже очищенный свинец?
Предлагаю вам сегодня подумать …
Кстати многие вытаскивают свинец для своих нужд, например кто-то заядлый рыболов и ему нужно делать грузила или мормышки для своих снастей, а зачем покупать, если у вас есть старая батарея.
Другие собирают опять новые аккумуляторы, скажем для нужд альтернативной энергетики и т.д., если покапать то применение можно увидеть во многих сферах, даже в краску стружку добавляют.
Но нам интересен вес, для начала давайте подумаем, из чего же вообще состоит полная конструкция.
Состав аккумулятора
Если вы думаете что свинец в батарее очищенный и оттягивает на себя больший вес, то вы мягко сказать – ошибаетесь.
Его очень мало применяют в чистых вариантах, в аккумуляторах для авто примерно 15 – 20%, а остальное идет в виде «оксидов». Если сказать обычными словами – то это соединения с другими элементами, зачастую и с другими металлами.
Также нужно учитывать вес пластикового корпуса, а также вес электролита (специальной токопроводящей жидкости).
Если разбить по процентной составляющей формула выходит примерно такая
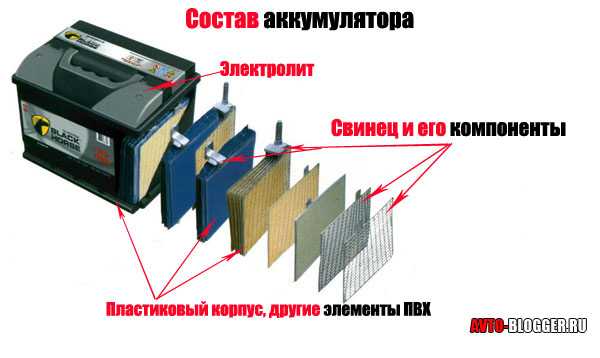
1) Свинец и его компоненты (оксиды и диоксиды) – порядка 60 – 70% от веса
2) Пластиковый корпус, перегородки и другие элементы ПВХ – 8 – 10%
3) Электролит (зачастую раствор серной кислоты) – 20%
Так что получается нормально – если брать вес обычного 55 Амперного варианта, а он составляет порядка 15 кг. То металла должно быть – 15Х0,7= 10,5 кг, ПВХ – 15Х0,1= 1,5 кг и соответственно, электролит – 15Х0,2 = 3 кг.

Вроде смысл есть, и переплавлять и использовать металл, но вот не все так просто! Сколько металла вы сможете получить при плавке, и разложатся ли диоксиды и прочие составляющие?
Плавим сами
Многие из нас привыкли плавить этот мягкий металл, на обычной плите у себя дома.

Некоторые мои друзья плавили на электрической плитке в гараже. Подойдет ли нам такая схема и сколько можно наплавить?
А вот не совсем!
В аккумуляторе чистого свинца, который легко поддается термической обработке (дом – гараж), всего – 15 – 20 %, это клеммы и «мостики», а также сама решетка, которая погружена в кислоту, а от нашей общей массы это всего – около 3 кг.

Остальной металл идет в качестве оксидов и диоксидов, что намного усложняет его добычу. Скажу так – нужно применять химические реактивы и более высокие температуры (от 600 градусов) чтобы разрушить это соединение! Поэтому многие из гаражных химиков списывают это на грязь или шлак, которого образуется примерно до 30 до 40 % от массы и просто его выкидывают, а это, кстати – около 5 килограмм.
Поэтому можно встретить в интернете много роликов что доля свинца в общей массе – мала, и не стоит его добывать таким способом. Особенно если вы планируете его, сдавать за деньги! Смотрим такой ролик.
В этом есть доля истины, но многие просто не могут его «готовить», то есть добывать, нет ни знаний, ни возможностей! Например – где вы найдете горелку с температурой в 600 – 1000 градусов, и сколько вам это будет стоить?
Самый легкий способ это сдавать неразобранную конструкцию в специальные пункты или на заводы изготовителя. Там есть и реактивы, и специально обученный персонал, да и плавильные печи присутствуют.
На этой ноте можно было бы заканчивать статью, однако я вам обещал разбивку по модификациям.
Сколько килограмм свинца в различных вариантах
Здесь я представлю несколько значений:
1) Общую массу с пластиком и кислотой.
2) Сколько можно добыть своими руками в гараже.
3) Сколько можно добыть на специальном оборудовании, на производстве.

55 А/ч
Общий вес – примерно 15 кг.
Чистый (можно добыть самому) – около 3 кг.
Общий в соединениях – 10,5 кг.
60 А/ч
Общий вес – примерно 17 кг.
Чистый – около 3,4 кг.
В соединениях – 11,9 кг.
75 А/ч
Общая масса – примерно 22 кг.
Чистый – 4,4 кг.
В соединениях – 15,4 кг.
90 А/ч
Масса около – 27 кг.
Очищенный – 5,4 кг.
Общий – 18,9 кг.
190 А/ч
Масса около – 43 кг.
Чистый – 8,6 кг.
В соединениях – 30,1 кг.
Теперь точно буду заканчивать, мораль проста – если хотите заработать, то несите неразобранный корпус в пункт приема, меньше мороки и больше денег заработаете!
Источник
zabarankoi.mirtesen.ru
Свинцово-кислотный аккумулятор — Википедия
Схема свинцово-кислотного аккумулятора при зарядке (слева) и при подключении потребителя электрического тока Схема расположения электродов в свинцово-кислотном аккумуляторе, пластины катода и анода располагаются попеременно с прослойкой изолятора и объединяется каждый токонесущей полоской в выводы аккумулятора Строение свинцово-кислотного аккумулятора: слева — пластины положительного электрода, изолятора из стекловаты, отрицательного электрода; справа — аккумулятор в сборе (извлечён из корпуса с электролитом). Пластины электродов представляют собой свинцовую (чаще сплав свинца и сурьмы для повышения механической прочности[1]) решётку, ячейки которой заполнены сульфатом свинца со связующим материалом, токонесущие полосы и выводы аккумулятора изготовлены из свинца Варианты электрода свинцово-кислотного аккумулятора Свинцово-кислотный аккумулятор в сборе
Свинцово-кислотный аккумулятор в сбореСвинцо́во-кисло́тный аккумуля́тор — тип аккумуляторов, получивший широкое распространение ввиду умеренной цены, неплохого ресурса (от 500 циклов и более), высокой удельной мощности. Основные области применения: стартерные аккумуляторные батареи в транспортных средствах, аварийные источники электроэнергии, резервные источники энергии. Строго говоря, аккумулятором называется один элемент аккумуляторной батареи, но в просторечии «аккумулятором» называют аккумуляторную батарею (сколько бы в ней ни было элементов).
Свинцовый аккумулятор изобрёл в 1859—1860 годах Гастон Планте, сотрудник лаборатории Александра Беккереля[2]. В 1878 году Камилл Фор усовершенствовал его конструкцию, предложив покрывать пластины аккумулятора свинцовым суриком. Русский изобретатель Бенардос применил покрытие губчатым свинцом для увеличения мощности батарей, которые использовал в своих работах со сваркой.
Принцип работы свинцово-кислотных аккумуляторов основан на электрохимических реакциях свинца и диоксида свинца в водном растворе серной кислоты.
При подключении к электродам аккумулятора внешней нагрузки начинается электрохимическая реакция взаимодействия оксида свинца и серной кислоты, при этом металлический свинец окисляется до сульфата свинца (в классическом варианте аккумулятора). Проведённые в СССР исследования показали, что при разряде аккумулятора протекает как минимум ~60 различных реакций, порядка 20 из которых протекают без участия кислоты электролита[3].
Во время разряда происходит восстановление диоксида свинца на катоде[3][4] и окисление свинца на аноде. При заряде протекают обратные реакции. При перезаряде аккумулятора, после исчерпания сульфата свинца, начинается электролиз воды, при этом на аноде (положительный электрод) выделяется кислород, а на катоде — водород.
Электрохимические реакции (слева направо — при разряде, справа налево — при заряде):
- PbO2+SO42−+4H++2e−⇆PbSO4+2h3O{\displaystyle PbO_{2}+SO_{4}^{2-}+4H^{+}+2e^{-}\leftrightarrows PbSO_{4}+2H_{2}O}
- Pb+SO42−−2e−⇆PbSO4{\displaystyle Pb+SO_{4}^{2-}-2e^{-}\leftrightarrows PbSO_{4}}
При разряде аккумулятора из электролита расходуется серная кислота и выделяется относительно более лёгкая вода, плотность электролита падает. При заряде происходит обратный процесс. В конце заряда, когда количество сульфата свинца на электродах снижается ниже некоторого критического значения, начинает преобладать процесс электролиза воды. Газообразные водород и кислород выделяются из электролита в виде пузырьков — так называемое «кипение» при перезаряде. Это нежелательное явление, при заряде его следует по возможности избегать, так как при этом вода необратимо расходуется, нарастает плотность электролита и есть риск взрыва образующихся газов. Поэтому большинство зарядных устройств снижает зарядный ток при повышении напряжения аккумулятора. Потери воды восполняют доливкой в аккумуляторы дистиллированной воды при обслуживании аккумуляторной батареи (некоторые автомобильные батареи не имеют открывающихся/отвинчивающихся пробок)[5].
Элемент свинцово-кислотного аккумулятора состоит из электродов и разделительных пористых пластин, изготовленных из материала, не взаимодействующего с кислотой, препятствующих замыканию электродов (сепараторов), которые погружены в электролит. Электроды представляют собой плоские решётки из металлического свинца. В ячейки этих решёток запрессованы порошки диоксида свинца (PbO2) — в анодных пластинах и металлического свинца — в катодных пластинах. Применение порошков увеличивает поверхность раздела электролит — твердое вещество, тем самым увеличивает электрическую ёмкость аккумулятора.
Электроды вместе с сепараторами погружены в электролит, представляющий собой водный раствор серной кислоты. Для приготовления раствора кислоты применяют дистиллированную воду.
Электрическая проводимость электролита зависит от концентрации серной кислоты и при комнатной температуре максимальна при массовой доле кислоты 35%[6], что соответствует плотности электролита 1,26 г/см³[7]. Чем больше проводимость электролита, тем меньше внутреннее сопротивление аккумулятора, и, соответственно, ниже потери энергии на нём. Однако, на практике в районах с холодным климатом применяются и более высокие концентрации серной кислоты, до 1,29−1,31 г/см³, это связано с тем, что при снижении концентрации из-за разряда электролит может замёрзнуть, а при замерзании образуется лёд, который может разорвать банки аккумулятора и повреждает губчатый материал пластин.
Существуют экспериментальные разработки аккумуляторов, где свинцовые решетки заменяют пластинами из переплетённых нитей углеродного волокна, покрытых тонкой свинцовой плёнкой. При этом используется меньшее количество свинца, распределённого по большой площади, что позволяет изготовить аккумулятор не только компактным и лёгким, при прочих равных параметрах, но и значительно более эффективным — помимо большего КПД, заряжается значительно быстрее традиционных аккумуляторов[8].
В аккумуляторах, применяемых в бытовых ИБП, систем охранной сигнализации и др. жидкий электролит загущают водным щелочным раствором силикатов натрия (Na2Si2O4) до пастообразного состояния. Это так называемые гелевые аккумуляторы (GEL), имеющие длительный ресурс. Другой вариант исполнения − с пористыми сепараторами из стеклоткани (AGM), допускающими более жёсткие режимы заряда[9].
Электрические и эксплуатационные параметры[править | править код]
- Удельная предельная теоретическая энергоёмкость (Вт·ч/кг): около 133.
- Удельная энергоёмкость (Вт·ч/кг): 25—40[10].
- Теоретическая удельная энергоплотность (Вт·ч/дм³): 1250[11].
- ЭДС одного заряжённого аккумулятора = 2,11—2,17 В, рабочее напряжение 2,1 В (3 или 6 аккумуляторов в итоге дают в батарее стандартные 6,3 В или 12,6 В соответственно)[3].
- Напряжение полностью разряженного аккумулятора = 1,75—1,8 В. Ниже разряжать их нельзя[3].
- Рабочая температура: от −40 °C до +40 °C.
- КПД: порядка 80—90 % (по току). КПД по энергии 70-80%[10].
Чаще всего свинцово-кислотные аккумуляторы применяются в составе аккумуляторной батареи с номинальным напряжением 6, 12 вольт, реже с другим кратным 2 напряжением. Промышленностью выпускаются варианты обслуживаемых (заливание электролита, дистиллированной воды, контроль плотности электролита, его замена) и не обслуживаемых в герметичном корпусе (исключается проливание электролита при изменений положения, переворачиваний) аккумуляторных батарей. Обслуживаемые аккумуляторные батареи могут выпускаться сухозаряженными (без залитого электролита), что увеличивает их срок хранения и не требует периодического обслуживания при хранении, заливка производится перед вводом в эксплуатацию[12].
Герметичная не обслуживаемая свинцово-кислотная аккумуляторная батарея напряжением 12 В и ёмкостью 4,5 А·ч бытовой электротехники
Свинцово-кислотные аккумуляторные батареи напряжением 8 В и ёмкостью 3,5 А·ч ИБП
Вариант обслуживаемой свинцово-кислотной аккумуляторной батареи для автомототракторной техники в эбонитовом корпусе, в подобных батареях была даже возможность заменить отдельный вышедший из строя аккумулятор
Вариант не обслуживаемой свинцово-кислотной аккумуляторной батареи для автомототракторной техники, нет доступа к заливным горловинам банок аккумуляторов
- Номинальная ёмкость, показывает количество электричества, которое может отдать данный аккумулятор. Обычно указывается в ампер-часах, и измеряется при разряде малым током (1/20 номинальной ёмкости, выраженной в А·ч)[13].
- Стартерный ток (для автомобильных аккумуляторов). Характеризует способности отдавать сильные токи при низких температурах. В большинстве случаев измеряется при −18 °C (0 °F) в течение 30 секунд. Различные методики замера отличаются (главным образом, допускаемым конечным напряжением) поэтому дают различные результаты[14].
- Резервная ёмкость (для автомобильных аккумуляторов) — характеризует время, в течение которого аккумулятор может отдавать ток 25 А до конечного напряжения 10,5 В согласно ГОСТ Р 53165-2008[15].
При эксплуатации «обслуживаемых» аккумуляторов (с открываемыми пробками на банках) на автомобиле при движении по неровной дороге неизбежно происходит просачивание электролита из-под пробок на корпус аккумулятора. Через электропроводную не высыхающую, из-за гигроскопичности, плёнку электролита происходит постепенный саморазряд аккумулятора. Во избежание глубокого саморазряда необходимо периодически нейтрализовать электролит протиранием корпуса аккумулятора, например, слабым раствором пищевой соды или разведённым в воде до консистенции жидкой сметаны хозяйственным мылом. Кроме того, особенно в жаркую погоду, происходит испарение воды из электролита; также количество воды в электролите уменьшается при перезаряде аккумулятора за счёт её электролиза. Потеря воды увеличивает плотность электролита, увеличивая напряжение на аккумуляторе. При существенной потере воды могут оголиться пластины, что одновременно увеличивает саморазряд и вызывает сульфатацию батареи. Поэтому необходимо следить за уровнем электролита и при необходимости доливать дистиллированную воду.
Эти меры вместе с проверкой автомобиля на паразитную утечку тока в его электрооборудовании и периодической подзарядкой аккумулятора могут существенно продлить срок эксплуатации аккумуляторной батареи.
Работа свинцово-кислотного аккумулятора при низких температурах[править | править код]
По мере снижения окружающей температуры параметры аккумулятора ухудшаются, однако, в отличие от прочих типов аккумуляторов, у свинцово-кислотных аккумуляторов это снижение относительно мало, что и обуславливает их широкое применение на транспорте. Эмпирически считается, что свинцово-кислотный аккумулятор теряет ~1 % отдаваемой ёмкости при снижении температуры на каждый градус от +20 °C. То есть, при температуре −30 °C свинцово-кислотный аккумулятор покажет примерно 50 % ёмкости.
Снижение ёмкости и токоотдачи при низких температурах обусловлено, в первую очередь, снижением скорости химических реакций (закон Аррениуса). Единственным способом повышения отдаваемой ёмкости является подогрев холодной батареи, как вариант — встроенным подогревателем (6СТ-190ТР-Н).
Разряженный аккумулятор в мороз может раздуться из-за замерзания электролита низкой плотности (близкой к 1,10 г/см3) и образования кристаллов льда, что приводит к необратимому повреждению свинцовых пластин внутри аккумулятора.
Низкие температуры электролита негативно влияют на работоспособность и зарядно-разрядные характеристики аккумулятора[16]:
- при температуре от 0 °C до −10 °C снижение зарядных и разрядных характеристик несущественно влияют на работоспособность аккумулятора;
- при температуре от −10 °C до −20 °C происходит снижение тока в стартерном режиме и ухудшение заряда;
- при температуре ниже −20 °C аккумуляторные батареи не обеспечивают надежного пуска двигателя и не способны принимать заряд от генератора.
Из-за большего внутреннего сопротивления, присущего современным аккумуляторам закрытого типа (т. н. «необслуживаемым», герметичным, герметизированным) при низких температурах по сравнению с обычными аккумуляторами (открытого типа), для них эти вопросы ещё более актуальны[17].
Для эксплуатации транспортных средств при очень низких температурах предназначены конструкции аккумулятора с внутренним электроподогревом[18].
Хранение[править | править код]
Свинцово-кислотные аккумуляторы следует хранить только в заряженном состоянии. При температуре ниже −20 °C подзаряд аккумуляторов должен проводиться постоянным напряжением 2,45 В/элемент 1 раз в год в течение 48 часов. При комнатной температуре — 1 раз в 8 месяцев постоянным напряжением 2,35 В/элемент в течение 6—12 часов. Хранение аккумуляторов при температуре выше 30 °C не рекомендуется.
Слой грязи, солей и плёнки электролита на поверхности корпуса аккумулятора создаёт проводник для тока между электродами и приводит к саморазряду аккумулятора, при глубоком разряде начинается преждевременная сульфатация пластин, и поэтому поверхность аккумулятора необходимо поддерживать в чистоте. Хранение свинцово-кислотных аккумуляторов в разряженном состоянии приводит к быстрой потере их работоспособности.
При длительном хранении аккумуляторов и разряде их большими токами (в стартерном режиме), или при уменьшении ёмкости аккумуляторов, нужно проводить контрольно-тренировочные циклы, то есть разряд-заряд токами номинальной величины.
При подготовке аккумуляторной батареи к зимнему хранению, что актуально для автомобилей не эксплуатируемых в холодное время года специалисты старейшей лаборатории НИИАЭ рекомендуют следующие действия:
1. Правильно и до конца зарядите аккумуляторную батарею. 2. Нанесите на положительный вывод АКБ пластичную смазку (литол, солидол и т. п.), так как плёнка электролита способна абсорбировать влагу из атмосферы, что может приводить к повышенному саморазряду. 3. Хранить аккумуляторы на холоде, так как при низких температурах саморазряд намного ниже. Электролит полностью заряженного аккумулятора начинает замерзать при температуре ниже −55 С.
В случае необходимости поездки в морозы следует перенести аккумулятор в отапливаемое помещение и в течение 7—9 часов (например, за ночь) он придёт в пригодное для пуска двигателя состояние.
Износ свинцово-кислотных аккумуляторов[править | править код]
При использовании технической серной кислоты и недистиллированной воды ускоряются саморазряд, сульфатация, разрушение пластин и уменьшение ёмкости аккумуляторной батареи[19].
При химических реакциях в аккумуляторе образуется плохо растворимое вещество — сульфат свинца PbSO4, осаждающийся на пластинах и создающий диэлектрический слой между электролитом и активной массой. Это один из факторов, снижающих срок службы свинцово-кислотной аккумуляторной батареи.
Основными процессами износа свинцово-кислотных аккумуляторов являются:
- сульфатация пластин[3], заключающаяся в образовании крупных кристаллов сульфата свинца, который препятствует протеканию обратимых токообразующих процессов;
- коррозия электродов, то есть электрохимические процессы окисления и растворения материала электродов в электролите, что вызывает осыпание материала электродов;
- слабая механическая прочность или плохое сцепление активной массы с электродными решётками, что приводит к опаданию активной массы[3][20];
- оползание и осыпание активной массы положительных электродов, связанное с разрыхлением, нарушением однородности[3].
Хотя батарею, вышедшую из строя по причине физического разрушения пластин, в домашних условиях восстановить нельзя, в литературе описаны химические растворы и прочие способы, позволяющие «десульфатировать» пластины. Простой, но чреватый полным отказом аккумулятора способ предполагает использование раствора сульфата магния[3]. Раствор сульфата магния заливается в секции, после чего батарею разряжают и заряжают несколько раз. Сульфат свинца и прочие остатки химической реакции осыпаются при этом на дно банок, это может привести к замыканию элемента, поэтому обработанные банки желательно промыть и заполнить новым электролитом номинальной плотности. Это позволяет несколько продлить срок использования устройства.
Кодовый символ, указывающий на то, что свинцовые батареи могут быть вторично переработаныВторичная переработка для этого вида аккумуляторов играет важную роль, так как свинец, содержащийся в аккумуляторах, является токсичным тяжёлым металлом и наносит серьёзный вред при попадании в окружающую среду. Свинец и его соли должны быть переработаны для возможности его вторичного использования.
Свинец из изношенных аккумуляторов используется для кустарной переплавки, например, при изготовлении грузил рыболовных снастей, охотничьей дроби или гирь. Кустарное извлечение свинца из аккумуляторов серьезно вредит как окружающей среде, так и здоровью плавильщиков, поскольку свинец и его соединения с парами и дымом разносятся по всей округе[21][22].
ru.wikipedia.org
Сколько свинца в аккумуляторе автомобиля?
Как известно, автомобильный аккумулятор содержит свинец. При этом многие автомобилисты, после того как источник электроэнергии в автомобиле выходит из строя, самостоятельно разбирают старый элемент питания как раз для того, чтобы добыть свинец. Для многих автолюбителей становится актуальным вопрос «Сколько свинца в аккумуляторе?».
Цель извлечения свинца из аккумулятора
Прежде чем начать повествование о способах извлечения свинца из аккумулятора, стоит определиться с тем, что можно дальше делать с извлеченным материалом. Во-первых, свинец достаточно высоко ценится в пунктах приема лома и цветных металлов, потому, сдав большое его количество, можно получить вполне приличную денежную сумму. Во-вторых, заядлые рыбаки из извлеченного металла плавят грузила, мотивируя свои действия тем, что не стоит платить за то, что и так имеется.
Некоторые даже добавляют стружку из свинца в краску для ее большей стойкости на окрашенной поверхности. Народные умельцы собирают новые аккумуляторные батареи, являющиеся своего рода альтернативным источником питания для определенных приборов и устройств.

Устройство автомобильного аккумулятора
Многие автолюбители уверены в том, что в конструкцию автомобильного аккумулятора входит чистый свинец, который и является причиной большого веса данного элемента питания. Однако это утверждение неверно.
На самом деле в аккумуляторе очень мало очищенного свинца, ориентировочно 15-20% от общей массы. Остальные 80-85% это оксиды (свинец «вперемешку» с другими элементами, а то и металлами). При этом нельзя забывать о том, что корпус из пластика также имеет свой вес. То же самое утверждение справедливо и для электролита (хорошо проводящей электричество жидкости), который используется в аккумуляторе.
Для того чтобы ответить на вопрос, сколько свинца в аккумуляторе, необходимо все составляющие аккумулятора разделить на компоненты и выразить их наличие в процентном соотношении.
Итак, в процентном соотношении состав в автомобильном аккумуляторе выглядит следующим образом:
- Свинец, а также оксиды и диоксиды: шестьдесят-семьдесят процентов от веса прибора.
- Электролит (наиболее часто в этом качестве используется раствор серной кислоты), от общей массы аккумуляторной батареи он занимает порядка двадцати процентов.
- Корпус из пластика, перегородки, и прочие элементы из ПВХ, порядка восьми – десяти процентов от общей массы аккумулятора.
Для большей наглядности в качестве примера стоит разобрать на компоненты 55-амперный аккумулятор. Он весит около пятнадцати килограмм. Металл занимает в таком аккумуляторе 10,5 килограмма, на пластик и ПВХ уходит полтора килограмма, остальное отдано электролиту – 3 килограмма.

Таким образом, с 55-амперного аккумулятора можно получить порядка 3-4 кг чистого свинца. Однако процесс переплавки достаточно непрост. Остаются открытыми темы, касающиеся фактического количества свинца после переплавки, а также разложения диоксидов на свинец и прочие компоненты. Поэтому вопрос, сколько свинца в аккумуляторе, по-прежнему остается открытым.
Сколько свинца в аккумуляторах различных «калибров»?
В нижеприведенной таблице дана масса аккумуляторов различной емкости. В верхней строке указана емкость аккумуляторов, во второй строке дано значение общего веса прибора для накопления энергии, в третьей строке можно отыскать долю свинца, которая находится в аккумуляторе в чистом виде, и его можно добыть. В четвертой колонке дана масса свинца вместе с оксидами и диоксидами.
55 А/ч | 60 А/ч | 75 А/ч | 90 А/ч | 190 А/ч |
15 кг | 17 кг | 22 кг | 27 кг | 43 кг |
Примерно 3 кг | Примерно 3,4 кг | Примерно 5,4 кг | Примерно 4,4 кг | Примерно 8,6 кг |
Доля свинца вместе с соединениями 10,5 кг | Доля свинца вместе с соединениями 11,9 кг | Доля свинца вместе с соединениями 15,4 кг | Доля свинца вместе с соединениями 18,9 кг | Доля свинца вместе с соединениями 30,1 кг |
Исходя их данных, которые представлены в вышеизложенной таблице, можно сделать вывод о том, что далеко не вся масса аккумулятора является чистым свинцом, и его процентная доля от общей массы аккумулятора ничтожно мала.
Сколько свинца в аккумуляторе 55 А/ч?
В аккумуляторной батарее на 55 А/ч находится десять с половиной килограммов свинца вместе с оксидами и диоксидами. Очищенного же металла получится всего лишь около трех килограмм. При этом примерно полтора килограмма весят пластиковый корпус и перегородки из ПВХ.

Поскольку общий вес чистого металла достаточно низок, разборка и добыча свинца из данного аккумулятора нецелесообразна. Времени и сил будет затрачено гораздо больше, чем можно выручить денег. Поэтому лучше всего аккумулятор занести в пункт приема металлолома.
Удельный вес свинца в аккумуляторе 60 А/ч
Если с аккумулятором в 55 А/ч все понятно, то сколько свинца в аккумуляторе 60 А/ч, и выгодно ли его добывать? В автомобильном аккумуляторе на 60 А/ч находится примерно двенадцать килограмм свинца и его примесей.
Если же говорить о чистом свинце, то в таком аккумуляторе его не больше трех-четырех килограмм. При этом остальная масса складывается из веса корпуса: пластмассы и перегородок ПВХ. Разница в удельном весе не является колоссальной, поэтому вывод напрашивается сам собой.
Как разобрать старый аккумулятор?
Перед тем как начать описывать процесс разборки старого аккумулятора, стоит отметить, что разборными делались аккумуляторы в СССР. На советском приборе можно было осуществить замену одной либо нескольких банок, и вновь собрать устройство.
Аккумуляторы, которые выпускаются в настоящее время, не предполагают вмешательства извне. Производитель создает эти устройства с расчетом на то, что после истечения срока их эксплуатации автомобилист избавится от вышедшего из строя элемента питания и приобретет новый.
Потому прежде чем собираться разбирать аккумулятор, следует потренироваться на нерабочем экземпляре. Также важно добавить и то, что после разборки и сборки аккумулятора его эксплуатация становится весьма и весьма большим вопросом.

Для разборки устройства необходимо вооружиться перчатками из резины, защитными очками, лобзиком, предназначенным для резки металла, болгаркой, пассатижами, молотком, плоской отверткой, зубилом, паяльником повышенной мощности, дрелью, а также строительным феном.
Аккумуляторы в основном заправляются кислотой, которая разведена дистиллированной водой до определенной плотности. Электролит при взаимодействии с кожей человека вызывает сильные химические ожоги. Для того чтобы обезопаситься от пагубного воздействия электролита, его нужно слить. Делается это посредством просверливания отверстий на дне банки. Вентиляцию банок надо предварительно закрыть. А под просверленные отверстия ставится стеклянная тара, туда и будет сливаться электролит. Если аккумуляторная батарея не оснащена пробками, то отверстия следует делать со стороны, где должны располагаться пробки. Так электролит вытечет гораздо быстрее.
После того как электролит был слит, нужно промыть банки водой. Дальше болгаркой либо лобзиком, следуя по периметру аккумулятора, отпиливается крышка от аккумуляторного корпуса. Затем следует потянуть за крышку. Вполне возможно, вместе с отпиленным элементом удастся вытащить аккумуляторные пластины. При этом крышка достаточно легко сойдет с приводных клемм. Если этого не произойдет, то придется поработать зубилом и молотком и вручную извлечь пластины аккумулятора.
После осуществления вышеперечисленных действий можно получить доступ к «внутренностям» аккумуляторной батареи.
Самостоятельная плавка свинца
Бытует распространенное мнение, что свинец из аккумуляторной батареи легко плавится в домашних условиях на плите: газовой или же электрической. Да, действительно, это так.

Но при этом плавится доступный металл: клеммы, мостики и решетка. Для того чтобы добыть остальной свинец, необходимо достичь температуры 600-1000 градусов и при этом использовать особые химические реагенты. Тем не менее в оксидах и диоксидах также присутствует свинец. Отвечая на вопрос, сколько свинца в аккумуляторе 55 А/ч, стоит учитывать не только легкоплавкий металл. Следует брать во внимание и тот, который можно получить из оксидов и диоксидов, используя реагенты и высокие температуры.
Так что вопросы, сколько чистого свинца в аккумуляторе и сколько свинца в нем в целом, имеют несколько разные ответы: первый ответ будет касаться металла, который легко получить и в домашних условиях. Второй — всего свинца, который находится в автомобильном аккумуляторе.
Целесообразно ли разбирать аккумулятор?
Исходя из вышеизложенного стоит ответить, что гораздо прибыльнее и эффективнее сразу же сдать аккумулятор в пункт приема или на завод-производитель. Таким образом, можно получить и больше денег (в сравнении с той суммой, которую можно получить за «свинцовые крохи»), и сэкономить время и силы.

Как определить количество свинца в аккумуляторе?
Для того чтобы узнать, сколько свинца в аккумуляторе, следует учитывать вес электролита, корпуса, а также свинца вместе с примесями других металлов.
Также можно просто воспользоваться представленной таблицей. В целом показатели количества этого металла в аккумуляторах различных марок примерно одинаковые. Поэтому если вопрос, сколько свинца в автомобильном аккумуляторе, по-прежнему не дает покоя, можно попытаться вычислить его вес самостоятельно.
Порядок вычисления
Для того чтобы узнать, сколько свинца в аккумуляторе автомобиля, следует из общей массы устройства вычесть вес электролита, а также перекрытий и корпуса. Масса всех этих деталей является неизменной составляющей всех батарей, поэтому порядок вычисления во всех случаях будет неизменным. После этих манипуляций можно узнать, сколько килограмм свинца в аккумуляторе.
Для выявления точного количества чистого металла необходимо учитывать и тот факт, что часть свинца в аккумуляторе находится с примесями. К примеру, решая задачу относительно того, сколько свинца в аккумуляторе 55 А/ч, можно ответить, что 3 кг. Но 1,5 килограмма в таком аккумуляторе занимают перегородки и корпус, а три килограмма электролит.
Для ответа на выше поставленные вопросы необходимо знать процентное соотношение свинца в аккумуляторе.
Меры предосторожности при разборке старого аккумулятора
Как упоминалось ранее, аккумулятор содержит достаточно агрессивное для окружающей среды вещество – электролит. Потому при разборке аккумулятора необходимо проявить максимальные аккуратность и точность. Необходимо использовать защитные очки, а также перчатки из плотной резины. При возможности лучше использовать защитный халат, хотя бы на этапе, когда происходит слив электролита.

Заключение
Подводя итоги вышесказанному, стоит отметить, что нет никакой необходимости разбирать аккумулятор для извлечения свинца. Тем более для того, чтобы сдать этот ценный металл в пункт приема лома.
Все дело заключается в том, что подавляющий процент свинца в аккумуляторе находится в виде оксидов и диоксидов, для расщепления на примеси и чистый металл требуется особое оборудование, высокие температуры и химикаты. Потому гораздо целесообразнее сдать целиковый аккумулятор в пункт приема старых приборов или же на завод-производитель. Этот шаг принесет гораздо больше денег при гораздо меньшей временной затрате.
К тому же ответ на вопрос, сколько кг свинца в аккумуляторе, не решит всех остальных сложностей. Разборка аккумулятора — дело непростое и опасное. В батарее имеется электролит, который способен вызвать сильнейшие химические ожоги.
Для того чтобы высчитать количество свинца в аккумуляторной батарее, необходимо лишь знать общее процентное соотношение свинца в аккумуляторе, как чистого, так и с примесями.
fb.ru
Автомобильный аккумулятор — Википедия
 Автомобильная свинцово-кислотная аккумуляторная батарея номинальной ёмкостью 40 А·ч, электрическое напряжение 12 В, «обратной» или «L» полярности, стандартные клеммы
Свинцово-кислотная аккумуляторная батарея трактора
Автомобильная свинцово-кислотная аккумуляторная батарея номинальной ёмкостью 40 А·ч, электрическое напряжение 12 В, «обратной» или «L» полярности, стандартные клеммы
Свинцово-кислотная аккумуляторная батарея трактора  Устройство автомобильной свинцово-кислотной аккумуляторной батареи на 12 В в разрезе. Батарея состоит из 6 аккумуляторов конструктивно объединённых в один общий корпус, каждый аккумулятор расположен в изолированной отдельной «банке»
Схематичное изображение свинцово-кислотной 12 вольтовой аккумуляторной батареи
Расположение электродов в «банке» свинцово-кислотного аккумулятора в составе аккумуляторной батареи
Устройство автомобильной свинцово-кислотной аккумуляторной батареи на 12 В в разрезе. Батарея состоит из 6 аккумуляторов конструктивно объединённых в один общий корпус, каждый аккумулятор расположен в изолированной отдельной «банке»
Схематичное изображение свинцово-кислотной 12 вольтовой аккумуляторной батареи
Расположение электродов в «банке» свинцово-кислотного аккумулятора в составе аккумуляторной батареиАвтомоби́льный аккумуля́тор (точнее — автомобильная аккумуляторная кислотная[источник не указан 282 дня] батарея [сокр. автомобильная АКБ] ) — тип электрической аккумуляторной батареи, применяемый на автомобильном или мототранспорте. Используется в качестве вспомогательного источника электроэнергии в бортовой сети при неработающем двигателе и для запуска двигателя.
На электротранспорте является не вспомогательным источником энергии, а основным. Такие аккумуляторы принято называть тяговыми.
Далее по тексту рассмотрена исключительно свинцово-кислотная аккумуляторная батарея, поскольку, если аккумулятор не тяговый, то как «автомобильный (стартёрный) аккумулятор», будет чаще использоваться такая. Замена пользователем на иной тип (к примеру, на литиевый блок) обычно невозможна[источник не указан 282 дня], даже при подходящем напряжении, в силу совершенно разных характеристик: прежде всего, свинцово-кислотные АКБ обладают уникальным свойством автоматической остановки заряда и резком росте напряжения, как и резком падении зарядного тока, при полном заряде. При этом, использование тех же литий-ионных или литий-железо-фосфатных аккумуляторов тоже возможно, но в силу того, что они требуют дополнительной электронной схемы для контроля за их состоянием, высокой стоимости, применяются реже[1][2][3].
На малотоннажных грузовиках, микроавтобусах и легковых автомобилях с дизельными двигателями используются аккумуляторы с электрическим напряжением 12 вольт.
- Напряжение без нагрузки (напряжение при снятых клеммах) аккумулятора можно связать с примерным уровнем заряда. Если аккумулятор находится на транспортном средстве, «напряжение без нагрузки» измеряется, когда двигатель остановлен, а нагрузка полностью отключена (сняты клеммы).
Степень заряженности оценивают на отключенном от нагрузки аккумуляторе, не менее, чем через 6 часов покоя, и при комнатной температуре. В случае температуры, отличной от комнатной, вносится температурная поправка. В среднем считается, что падение температуры на 1 °C от комнатной снижает ёмкость примерно на 1 %, таким образом при −30 °C ёмкость автомобильной АКБ будет равна примерно половине от ёмкости при +20 °C.
| Напряжение без нагрузки при T = 26,7 °C | Примерный заряд | Плотность электролита при T = 26,7 °C | |
|---|---|---|---|
| 12 В | 6 В | ||
| 12,65 В | 6,32 В | 100 % | 1,265 г/см³ |
| 12,35 В | 6,22 В | 75 % | 1,225 г/см³ |
| 12,10 В | 6,12 В | 50 % | 1,190 г/см³ |
| 11,95 В | 6,03 В | 25 % | 1,155 г/см³ |
| 11,70 В | 6,00 В | 0 % | 1,120 г/см³ |
- Напряжение без нагрузки также зависит от температуры и от плотности электролита при полном заряде. Следует заметить, что плотность электролита при одном и том же уровне заряда в свою очередь также зависит от температуры (обратная зависимость).
- Ёмкость аккумулятора, измеряющаяся в ампер-часах. Применительно к маркировке аккумулятора, значение ёмкости показывает, каким током будет равномерно разряжаться автомобильная АКБ до конечного напряжения при 20-часовом цикле разряда. Например, обозначение 6СТ-60 означает, что батарея в течение 20 часов будет отдавать ток 3 А, при этом в конце напряжение на клеммах не упадет до 10,5 В. Однако, это вовсе не означает линейную зависимость времени разряда от разрядного тока. Целый час стабильно отдавать 60 А наша батарея не сможет.
Особенностью аккумуляторов является уменьшение времени разряда с повышением разрядных токов. Зависимость времени разряда от тока разряда близка к степенной. Распространена, в частности, формула немецкого ученого Пейкерта (англ.), который установил, что: Cp=Ikt,{\displaystyle C_{p}=I^{k}t,}. Здесь Cp{\displaystyle C_{p}} — ёмкость аккумулятора, а k{\displaystyle k} — число Пейкерта — показатель степени, постоянный для данного аккумулятора или типа аккумуляторов. Для свинцовых кислотных аккумуляторов число Пейкерта обычно изменяется от 1,15 до 1,35. Величину константы в левой части уравнения можно определить по номинальной ёмкости аккумулятора. Тогда, после нескольких преобразований, получим формулу для реальной ёмкости аккумулятора E{\displaystyle E} при произвольном токе разряда I{\displaystyle I}:
E=En(InI)p−1{\displaystyle E=E_{n}\left({\frac {I_{n}}{I}}\right)^{p-1}}.
Здесь En{\displaystyle E_{n}} — номинальная ёмкость аккумулятора, а In{\displaystyle I_{n}} — номинальный ток разряда, при котором задана номинальная ёмкость (обычно ток 20-часового или 10-часового цикла разряда).
Ёмкость аккумулятора, как правило, выбирается исходя из рабочего объёма двигателя (больший объём — бо́льшая мощность стартёра — бо́льшая ёмкость АКБ), его типа (для дизельных ёмкость автомобильной АКБ должна быть больше, чем для бензиновых при равном объёме цилиндров) и условий эксплуатации (для районов с холодным климатом ёмкость увеличивают, по причине снижения ёмкости АКБ при отрицательных температурах и затруднения пуска двигателя стартёром из-за загустения масла).
- Резервная ёмкость. В отличие от номинальной ёмкости, которая определяется разрядом относительно малым током, резервная ёмкость показывает, сколько времени способен проехать автомобиль зимней ночью при неисправности генератора. Ток разряда принимается равным 25 А, поскольку зимней ночью очень много энергии уходит на освещение и обогрев салона. При этом нельзя просто разделить номинальную ёмкость автомобильной АКБ на 25 А. При таком токе резервная ёмкость составит примерно 2/3 от номинальной. Как правило, значение резервной ёмкости указывается на маркировке автомобильной АКБ в минутах.
- Пусковой ток. Или ток холодной прокрутки (cold cranking amps CCA). Максимальный ток, который способен отдавать аккумулятор без посадки напряжения на клеммах ниже 9В в течение 30 секунд при −18 °C по ГОСТ 53165-2008.
- При температуре окружающего воздуха –10 °C зарядные характеристики аккумулятора, не имеющего обогрева, из-за охлаждения ухудшаются, а при температуре ниже –30 °C заряд от штатного генератора автомобиля практически отсутствует[4]. Температура электролита в аккумуляторе, установленном на автомобиле, на 5—7 °C выше температуры окружающей среды и изменяется вслед за ней с запаздыванием на 4—5 часа. В режиме длительного движения за 10—12 часов температура электролита в не обогреваемых аккумуляторных батареях повышается на 2—3 °C, а при наличии обогреваемого отсека для аккумуляторных батарей на 5—7 °C. Поэтому, для надёжной эксплуатации в условиях низких температур применяются конструкции аккумулятора с внутренним электроподогревом[5][6].
Аккумулятор автомобиля содержит химические вещества, которые при взаимодействии производят электрический ток. Два разнородных металла помещаются в кислотную среду, которая называется электролитом. Возникает поток электронов и электроны из одной группы пластин переходят в другую.
Батарея заряжена
Полностью заряженная батарея содержит отрицательную пластину губчатого свинца (Pb) — катод, положительную пластину диоксида свинца (PbO2) – анод, и электролит из раствора серной кислоты (H2SO4) и воды (H2O).
Батарея разряжается
Когда аккумулятор разряжается, диоксид свинца на катоде восстанавливается, на аноде свинец окисляется. Металлы обоих пластин вступают в реакцию с SO4, в результате образуется сульфат свинца (PbSO4). Водород (H2) из серной кислоты вступает в реакцию с кислородом (O2) из положительной пластины и образуется вода (H2O). При этом расходуется серная кислота и образуется вода. Правильная зарядка во многом определяет ресурс службы батареи.[7]
Батарея разряжена
В полностью разряженном аккумуляторе обе пластины покрыты сульфатом свинца (PbSO4), а электролит разбавлен до большей степени водой (H2O).
Батарея заряжается
Автомобильный аккумулятор после взрываПроцесс противоположен разрядке.
Сульфат (SO4) покидает пластины и объединяется с водородом (H2), превращаясь в серную кислоту (H2SO4). Свободный кислород (O2) объединяется со свинцом (Pb) на положительной пластине с образованием диоксида свинца (PbO2). Когда батарея приближается к полной зарядке, водород образуется на отрицательных пластинах, а кислород — на положительных, происходит газообразование. Выделяющийся газ взрывоопасен.
- Тип батареи
В основном используется свинцово-кислотный тип. Собственно батарея состоит из 6 аккумуляторов (банок), каждая номинальным напряжением около 2,2 вольта, соединённых последовательно в батарею. Обычный электролит представляет собой смесь дистиллированной воды и серной кислоты с плотностью в пределах 1,23-1,31 г/см³ (чем больше плотность электролита, тем более морозостойкая батарея), но сейчас появились автомобильные АКБ построенные на базе технологии AGM (Absorbent Glass Mat), электролит в которых абсорбирован в стеклянном волокне[уточнить], а также т. н. гелевые аккумуляторы, где электролит загущается до гелеобразного состояния силикагелем (технология носит название GEL).
- Размеры
Так сложилось, что при разработке нового типа или даже марки автотехники нередко приходилось разрабатывать под неё новую автомобильную АКБ. В дальнейшем производители разработали большую номенклатуру различных аккумуляторов, существенно различающихся типоразмерами и электрическими характеристиками. Для тяжёлых грузовиков и спецмашин, имеющих бортовую сеть 24 вольта, применяются две одинаковые 12-вольтовые батареи, соединённые последовательно или одна 24-вольтовая батарея (редко).
В настоящее время существует несколько форм-факторов батарей. Аккумуляторы для японского и европейских рынков могут иметь разные размеры.
- Полярность
«Обратная» или «прямая». Определяет расположение электродов на корпусе автомобильной АКБ. Для автомобилей отечественного выпуска характерна прямая полярность, при которой плюсовая клемма находится слева, а минусовая — справа, при положении аккумулятора «клеммы ближе к вам». Установить чужую батарею, например «европейскую» на японский автомобиль, зачастую бывает невозможно. Может потребоваться удлинение проводов.
- Диаметр контактных клемм
В типе Euro — type 1 — 19,5 мм «плюсовая» клемма и 17,9 мм «минусовая» клемма. Тип Asia — Type 3 — 12,7 мм у «плюсовой» клеммы, — и 11,1 мм у клеммы «минус»[8]. Выпускаются «колпачки» — переходники с тонких клемм на толстые.
- Тип крепления
В конкретном транспортном средстве может быть реализован один из типов крепления автомобильной АКБ — верхнее или нижнее. В ряде автомобилей конструкции для закрепления батареи может быть не предусмотрено. Обозначения типов нижнего крепления следующие: B00, B01, B03, B13.
- Необходимость обслуживания
По этому принципу автомобильные АКБ классифицируют на два типа: обслуживаемые (и как их подкатегория — малообслуживаемые) и необслуживаемые (в тексте ГОСТа обозначенные как безуходные). В простых по конструкции аккумуляторах необходим регулярный контроль состояния электролита и регулярная подзарядка по специальной технологии с помощью стационарного зарядного устройства. На промышленных предприятиях для ухода за автомобильными аккумуляторами есть специально обученные люди (аккумуляторщики) а также зарядные станции.
Однако «необслуживаемые» автомобильные АКБ — это не значит, что за такой батареей совсем не нужен уход. Как правило, необслуживаемая батарея имеет встроенный индикатор-ареометр, по цвету которого определяется плотность электролита — зелёный поясок при нормальной плотности, красный или белый — при низкой (батарея подлежит замене). Также необходимо периодически контролировать уровень электролита по меткам на корпусе. На всех автомобильных АКБ во избежание повреждения аккумуляторного отсека кислотой необходимо контролировать герметичность корпуса, заливных пробок и чистоту дренажных отверстий, а при появлении признаков электролита устранить течь и тщательно промыть корпус и отсек автомобильной АКБ нейтрализующим щелочным составом. Также необходимо периодически тщательно очищать и смазывать клеммы литиевой смазкой, во избежание их электрокорозийного разрушения.
- Различные типы аккумуляторов обладают разными особенностями, которые не позволяют однозначно назвать «лучший» тип аккумулятора. Можно говорить только о лучшей применимости различных типов аккумуляторов в разных условиях. Так, например, современные «кальциевые» аккумуляторы обладают низким саморазрядом, не требуют обслуживания, однако не терпят глубоких разрядов, например, при коротких поездках в зимние морозы, или длительной стоянке автомобиля. В то же время, для «обслуживаемых» (практически не производятся) и «малообслуживаемых» аккумуляторов глубокий разряд не столь губителен, зато такие типы аккумуляторов требуют доливки дистиллированной воды (при исправном электрооборудовании и среднем пробеге — примерно 1 раз в 4—7 месяцев).
- С понижением температуры падает способность аккумулятора «принимать заряд». Поэтому короткие поездки в зимние морозы, особенно с включёнными фарами, могут довольно быстро привести к полному разряду даже абсолютно исправного аккумулятора. Это приводит не только к невозможности запуска мотора, но и к сокращению срока службы аккумулятора, особенно «кальциевого».
- Зимой аккумулятор рекомендуется периодически снимать с автомобиля и заряжать зарядным устройством после согревания на воздухе до положительной температуры. Согревать холодный аккумулятор в горячей воде нежелательно по причине возможного частичного осыпания активной массы пластин из-за быстрых температурных деформаций.
- Существует мнение[где?] о недопустимости установки на автомобиль аккумулятора с повышенной ёмкостью, так как при большей ёмкости автомобильная АКБ якобы не будет успевать заряжаться. Однако, энергия, потраченная на пуск двигателя, не зависит от ёмкости, поэтому при исправном генераторе будет восполнена в автомобильной АКБ за одно и то же время. Также опасение у некоторых вызывает возможность сгорания стартера, однако потреблённый стартером ток зависит не от ёмкости автомобильной АКБ, а только от его внутреннего сопротивления и условий пуска. Для районов с суровыми зимами рекомендуется установка автомобильной АКБ повышенной ёмкости. При этом аккумулятор способен будет отдать больший ток при пуске, увеличивается количество попыток пуска, уменьшается относительный разряд батареи, что увеличивает надёжность и продлевает срок службы[9]. Однако, у менее ёмкого аккумулятора скорее всего просадка напряжения в момент пуска двигателя больше, чем у более ёмкого, а значит и возможный максимальный ток тоже меньше, чем у более ёмкого, так что, возможно, доля правды в этом мифе всё-таки присутствует. Однако, следует иметь в виду, что аккумулятор большей ёмкости (нежели штатный) требует и большего времени для полной зарядки, если он сильно разряжен. А это случается зимой довольно часто, так как такой аккумулятор позволяет долго крутить стартер. Также, чем больше ёмкость, тем желательнее больший зарядный ток. Особенностью свинцово-кислотных аккумуляторов является то, что они сильно снижают свой ресурс, если заряжены не на 100 %, вследствие возникающей необратимой сульфатации. Поэтому, если в зимнее время аккумулятор с большей ёмкостью будет всё-таки сильно разряжен долгими попытками пуска, то вероятность выхода его из строя будет выше из-за нехватки времени на полный восстановительный заряд, что в ряде случаев усугубится также недостаточно сильным током, выдаваемым штатным генератором, особенно в режиме холостого хода. Следовательно, для продления ресурса аккумулятора большей ёмкости зимой следует его периодически снимать, отогревать и заряжать. Иначе, постоянно недозаряженный аккумулятор прослужит недолго, и единственным плюсом его применения будет увеличенное время прокрутки мотора и величина стартового тока, которые начнут неуклонно уменьшаться вследствие сульфатации, вплоть до полной непригодности аккумулятора. Также следует учитывать, что аккумулятор существенно бо́льшей ёмкости будет иметь бо́льшие габаритные размеры и может не поместиться в отсеке для аккумуляторной батареи. В интернете можно встретить утверждение, что в условиях низких температур зимой процесс сульфатации пластин происходит крайне медленно в силу особенностей прохождения химической реакции, однако следует критически относиться к этому утверждению, так как в процессе работы аккумулятор нагревается, и, следовательно, сульфатация всё же имеет место.
- Крайне нежелательно заменять аккумулятор при работающем двигателе, поскольку связанные с отключением и подключением аккумулятора скачки напряжения могут вывести из строя электрооборудование автомобиля. При необходимости замены аккумулятора при работающем двигателе, для минимизации скачка напряжения необходимо перед отключением аккумулятора включить в автомобиле максимальное количество электроприборов (фары, мотор «печки», магнитолу, обогрев заднего стекла и т. д.). Подключение каждой клеммы должно производиться быстро, без многократного касания клеммой вывода аккумулятора. Обороты двигателя не должны превышать холостых. В идеале отключаемый/подключаемый аккумуляторы и клеммы автомобиля необходимо временно соединить параллельно проводами, после чего отсоединить все провода от отключаемого аккумулятора, установить подключаемый, надеть на него клеммы, и в самом конце отсоединить временные провода от клемм автомобиля и от подключённого аккумулятора. Таким образом достигается заведомо постоянное соединение какого-либо из аккумуляторов, и практически нивелируются нежелательные скачки напряжения.
- При севшем аккумуляторе, т. н. «прикуривание» от другой автомашины необходимо осуществлять с тщательным соблюдением определённого набора правил, определяемых производителем автомобиля. Нарушение этих правил может оказаться причиной выхода из строя оборудования автомобиля.
ru.wikipedia.org

 Защитные очки и резиновые перчатки.
Защитные очки и резиновые перчатки.